环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
ΔH1=100.3 kJ·mol −1 ①
H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1 ②
对于反应: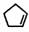 (g)+ I2(g) =
(g)+ I2(g) = (g)+2HI(g) ③ ΔH3=___________kJ·mol −1。
(g)+2HI(g) ③ ΔH3=___________kJ·mol −1。
2.某温度下,等物质的量的碘和环戊烯( )在刚性容器内发生反应③,起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为_________,该反应的平衡常数Kp=_________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有__________(填标号)。
)在刚性容器内发生反应③,起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为_________,该反应的平衡常数Kp=_________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有__________(填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
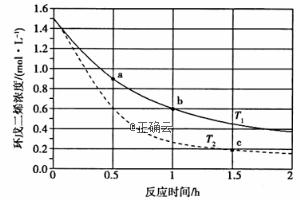
3.环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。
A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L−1
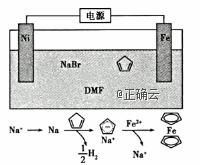
4.环戊二烯可用于制备二茂铁(Fe(C5H5)2结构简式为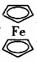 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
该电解池的阳极为____________,总反应为__________________。电解制备需要在无水条件下进行,原因为_________________________。
答案
1.89.3;
2.40%;3.56×104;BD
3.CD;
4.Fe电极;Fe+2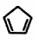 =
=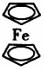 +H2↑[Fe+2C5H6=Fe(C5H5)2+H2↑];水会阻碍中间物Na的生成;水会电解生成OH−,进一步与Fe2+反应生成Fe(OH)2
+H2↑[Fe+2C5H6=Fe(C5H5)2+H2↑];水会阻碍中间物Na的生成;水会电解生成OH−,进一步与Fe2+反应生成Fe(OH)2
解析:1.根据盖斯定律①-②,可得反应③的ΔH=89.3KJ/mol;
2. 平衡时总压增加了20%,即气体总物质的量增加了20%。设碘和环戊烯的初始投料均为x mol,平衡时环戊烯的转化量为Δx mol,则平衡时体系中气体总物质的量增加了Δx mol,Δx mol =2x×20%=0.4x,环戊烯的转化率=Δx/x×100%=0.4x/x×100%=40%;起始总压为
105 Pa,平衡总压为1.2×105 Pa,可得出平衡时I2、 、
、 、HI的分压依3×104 Pa、3×104 Pa、2×104 Pa、4×104 Pa,Kp=
、HI的分压依3×104 Pa、3×104 Pa、2×104 Pa、4×104 Pa,Kp=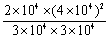 Pa≈3.56×104Pa。A项,通入惰性气体增加了体系总压强,但本质上未改变相关气体的分压,气体浓度不变,平衡不移动,环戊烯平衡转化率不变,故错误;B项,该反应是吸热反应,提高温度平衡正向移动,环戊烯平衡转化率增加,故正确;C项,增加环戊烯浓度可以使平衡正向移动,但环戊烯平衡转化率降低,故错误;D项,增加碘浓度可以使环戊烯的平衡转化率增加,故正确。
Pa≈3.56×104Pa。A项,通入惰性气体增加了体系总压强,但本质上未改变相关气体的分压,气体浓度不变,平衡不移动,环戊烯平衡转化率不变,故错误;B项,该反应是吸热反应,提高温度平衡正向移动,环戊烯平衡转化率增加,故正确;C项,增加环戊烯浓度可以使平衡正向移动,但环戊烯平衡转化率降低,故错误;D项,增加碘浓度可以使环戊烯的平衡转化率增加,故正确。
3.A项,观察不同温度下曲线的变化趋势,不难发现T2时反应更快,则T2>T1故错误;B项,a点对应温度低于c点对应温度,但a点环戊二烯浓度大于c点环戊二烯的浓度,故v(a)与v(c)大小无法确定,故错误;C项,v(a,正)>v(a,逆),v(b,正)>v(b,逆),又v(a,正)>v(b,正),则v(a,正)必然大于v(b,逆),故正确;D项,由图像可知b点环戊二烯的浓度为0.6 mol•L-1,环戊二烯转化的浓度=1.5 mol•L-1-0.6 mol•L-1=0.9 mol•L-1,则生成的二聚体的浓度=0.9 mol•L-1×1/2=0.45 mol•L-1,故正确。
4.根据反应历程可知,铁电极溶解生成了Fe2+,故应让Fe电极作电解池的阳极;由反应历程可知,反应物为Fe与环戊二烯,生成物为二茂铁和H2,再根据原子守恒写出总反应式;根据反应历程中有Na生成,水会与Na反应,从而中止反应,且电解过程中水会在阴极生成OH-,进一步与Fe2+反应生成Fe(OH)2。









 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号